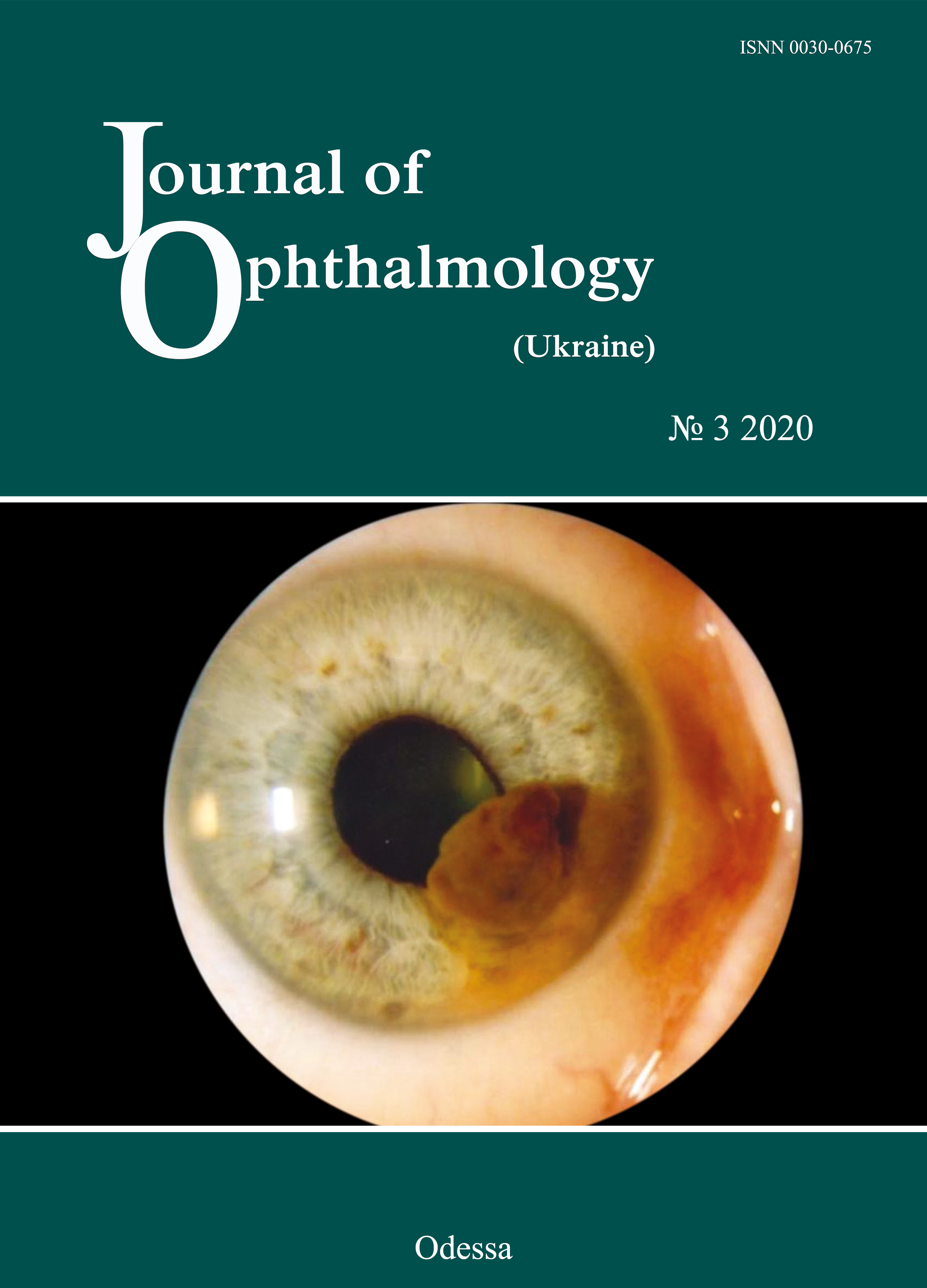
Динаміка депонування та дифузії лікарських препаратів (хлоргексидин, 5 фторурацил і доксорубіцин) при використанні гідрогелевих імплантатів з різною щільністю
DOI:
https://doi.org/10.31288/oftalmolzh202035360Ключові слова:
гібридний гідрогель, ендопротезування, депонування і дифузія лікарських препаратів, ступінь щільності гідрогелів, реконструктивні операціїАнотація
Актуальність. У зв'язку з явною тенденцією до росту очного травматизму, зростає кількість відновлюючих операцій на орбіті та окулоорбітальній ділянці, що потребує імплантуючих матеріалів. Слід зазначити, що важливим моментом є запобігання виникнення навколо імплантату запальної реакції, а після видалення злоякісної пухлини її рецидиву, у зв’язку з цим важливо, щоб імплантуючі матеріали містили в собі протимікробні та протипухлинні лікарські препарати.
Мета – вивчити динаміку депонування та дифузію лікарських препаратів (хлоргексидин, 5 фторурацил і доксорубіцин) при використанні гідрогелевих імплантатів з різною щільністю.
Матеріал та методи. Фармакопрепарати: 2,0% водний розчин хлоргексидину біглюконату. 5 фторурацил «Ебеве» – концентрат для розчину для інфузій, що містить 50 мг/мл, доксорубіцин – концентрат для розчину для інфузій, що містить 2 мг/мл.
Результати. Нами встановлено, що кінетика дифузії лікарських препаратів з рідко-зшитого гідрогелю досягає мінімального терапевтичного рівня уже протягом кількох хвилин, тоді як у випадку щільно-зшитого гідрогелю дифузія розпочинається із затримкою на кілька годин. Також було відмічено, що щільно-зшитий гідрогель має вищу здатність до депонування препаратів (хлоргексидин і 5 фторурацил), а отже, його доцільно використовувати для імплантатів з пролонгованим антибактеріальним ефектом, тоді як рідко-зшитий гідрогель – для термінового викиду ударної дози антисептику. Вказаний гідрогель забезпечує у експериментах in vitro у 3-4 рази більшу концентрацію в оточуючому середовищі у порівнянні зі щільно-зшитим полімером, а також забезпечує більш плавне, пролонговане вивільнення лікарського препарату.
Висновок. Така пролонгуюча здатність гібридних гідрогелевих імплантатів сприятиме їх застосуванню для депонування протипухлинних препаратів і підтримання їх ефективної концентрації в патологічному вогнищі.
Посилання
1.O.V. Grusha, Ia.O. Grusha. [Five hundred of orbital plastic repairs: analysis of complications]. Vestn Oftalmol. Jan-Feb 2006;122(1):22-4. Russian.
2.Gundorova RA, Neroev VV, Kashnikov VV, editors. [Ocular injuries]. Moscow: GEOTAR-Media; 2009. Russian.
3.Krasnovid TA. [Ocular trauma under present conditions. Providing urgent care in Ukraine]. Proceedings of the Conference of Ophthalmologists of Chernihiv, Kyiv, and other regions. Chernihiv; 2013. pp. 40-4. Russian.
4.Tselomudryi OI, Venger GE, Rizvaniuk AV, Pogorelyi DN, Putienko VA. [Current system of stage-by-stage treatment for combat-related eye injuries in the area of ATO]. In: [Proceedings of the Conference commemorating the 80th anniversary of the Filatov Institute and 14th Congress of the Black Sea Ophthalmological Society]. Odesa, 2016. Russian.
5.Maletskiy AP, Samchenko Iu.M, Vit VV, Bigun NM, Kernosenko LO. [Response of orbital and auricular soft tissues to the developed hydrogel implant in rabbits]. Arkhiv oftalmologii Ukrainy. 2018;6(2):20-7. Ukrainian.https://doi.org/10.22141/2309-8147.6.2.2018.172220
6.Chai Q, Jiao Y, Yu X. Hydrogels for biomedical applications: Their characteristics and the mechanisms behind them. Gels. 2017;3(1):6.https://doi.org/10.3390/gels3010006
7.Wichterle O, Lim D. Hydrophilic gels for biological use. Nature. 1960; 185: 117-8.https://doi.org/10.1038/185117a0
8.Hoare TR, Kohane DS. Hydrogels in drug delivery: Progress and challenges. Polymer. 2008;49: 1993-2007.https://doi.org/10.1016/j.polymer.2008.01.027
9.Jeong CG, Zhang H, Hollister SJ. Three-dimensional poly (1,8-octanediol-co-citrate) scaffold pore shape and permeability effects on sub-cutaneous in vivo chondrogenesis using primary chondrocytes. Acta Biomater. 2011 Feb;7(2):505-14.https://doi.org/10.1016/j.actbio.2010.08.027
10.Murray RZ, West ZE, Cowin AJ, Farrugia BL. Development and use of biomaterials as wound healing therapies. Burns Trauma. 2019;7:2.https://doi.org/10.1186/s41038-018-0139-7
11.Overstreet DJ, McLemore RY, Doan BD, Farag A, Vernon BL. Temperature-responsive graft copolymer hydrogels for controlled swelling and drug delivery. Soft Matter. 2013; 11: 294-304. https://doi.org/10.1080/1539445X.2011.640731
12.Yu X, Jiao Y, Chai Q. Applications of gold nanoparticles in biosensors. Nano LIFE. 2016; 6: 1642001.https://doi.org/10.1142/S1793984416420010
13.Sugak OA, Panasenko OI, Knysh YG, Kamyshny OM. [Antimicrobial and antifungal activity of derivatives of 3- (alkylthio) -4-R-5- (thiophen-2-ylmethyl) - 4H-1,2,4-triazoles]. Aktualni pytannia farmacevtychnoi i medychnoi nauky ta praktyky. 2015;3(19):67-70. Ukrainian.
14.Shapiro JM, Oyen ML. Hydrogel composite materials for tissue engineering scaffolds. JOM. 2013; 65: 505-16.https://doi.org/10.1007/s11837-013-0575-6
15.Kryklia SO, Samchenko Iu.M, Konovalova VV, Poltoratska TP, Pasmurtseva NO, Ulberg ZR. [Hybrid Ph- and thermosensitive hydrogels based on polyvinylalcohol and acrylic monomers]. Magisterium. 2016;63:20-8. Ukrainian.
16.Br?nler R, Aibibu D, W?ltje M, Anthofer AM, Cherif C. In silico modeling of structural and porosity properties of additive manufactured implants for regenerative medicine. Mater Sci Eng C Mater Biol Appl. 2017; 76: 810-817.https://doi.org/10.1016/j.msec.2017.03.105
17.Abureesh MA, Oladipo AA, Gazi M. Facile synthesis of glucose-sensitive chitosan-poly(vinyl alcohol) hydrogel: drug release optimization and swelling properties. Int J Biol Macromol. 2016 Sep;90:75-80.https://doi.org/10.1016/j.ijbiomac.2015.10.001
18.Van Tienen TG, Heijkants RG, Buma P, de Groot JH, Pennings AJ, Veth RP. Tissue ingrowth and degradation of two biodegradable porous polymers with different porosities and pore sizes. Biomaterials. 2002 Apr;23(8):1731-8.https://doi.org/10.1016/S0142-9612(01)00280-0
19.Yang S, Leong KF, Du Z, Chua CK. The design of scaffolds for use in tissue engineering. Part I. Traditional factors. Tissue Eng. 2001 Dec;7(6):679-89.https://doi.org/10.1089/107632701753337645
20.Zeltinger J, Sherwood JK, Graham DA, M?eller R, Griffith LG. Effect of pore size and void fraction on cellular adhesion, proliferation, and matrix deposition. Tissue Eng. 2001 Oct;7(5):557-72.https://doi.org/10.1089/107632701753213183
21.Oh SH, Park IK, Kim JM, Lee JH. In vitro and in vivo characteristics of PCL scaffolds with pore size gradient fabricated by a centrifugation method. Biomaterials. 2007 Mar;28(9):1664-71.https://doi.org/10.1016/j.biomaterials.2006.11.024
22.Murphy CM, Haugh MG, O'Brien FJ. The effect of mean pore size on cell attachment, proliferation and migration in collagen-glycosaminoglycan scaffolds for bone tissue engineering. Biomaterials. 2010 Jan;31(3):461-6.https://doi.org/10.1016/j.biomaterials.2009.09.063
23.Bulysheva AA, Bowlin GL, Klingelhutz AJ, Yeudall WA. J. Low-temperature electrospun silk scaffold for in vitro mucosal modeling. Biomed Mater Res. Part A. 2012; 100: 757-67.https://doi.org/10.1002/jbm.a.33288
24.Rnjak-Kovacina J, Wise SG, Li Z, Maitz PK, Young CJ, Wang Y, Weiss AS. Tailoring the porosity and pore size of electrospun synthetic human elastin scaffolds for dermal tissue engineering. Biomaterials. 2011 Oct;32(28):6729-36.https://doi.org/10.1016/j.biomaterials.2011.05.065
25.Somo SI, Akar B, Bayrak ES, Larson JC, Appel AA, Mehdizadeh H, Cinar A, Brey EM. Pore interconnectivity influences growth factor mediated vascularization in sphere-templated hydrogels. Tissue Eng Part C Methods. 2015 Aug;21(8):773-85.https://doi.org/10.1089/ten.tec.2014.0454
26.Khare A, Peppas NA. Swelling/deswelling of anionic copolymer gels. Biomaterials. 1995 May;16(7):559-67.https://doi.org/10.1016/0142-9612(95)91130-Q
27.Gamelin EC, Danquechin-Dorval EM, Dumesnil YF, et al. Relationship between 5-fluorouracil (5-FU) dose intensity and therapeutic response in patients with advanced colorectal cancer receiving infusional therapy containing 5-FU. Cancer. 1996 Feb 1;77(3):441-51.https://doi.org/10.1002/(SICI)1097-0142(19960201)77:3<441::AID-CNCR4>3.0.CO;2-N
28.Parker WB, Cheng YC. Metabolism and mechanism of action of 5-fluorouracil. Pharmacol Ther. 1990;48(3):381-95.https://doi.org/10.1016/0163-7258(90)90056-8
29.Wang LL, Huang S, Guo HH, Han YX, Zheng WS, Jiang JD. In situ delivery of thermosensitive gel-mediated 5-fluorouracil microemulsion for the treatment of colorectal cancer. Drug Des Devel Ther. 2016 Sep 8;10:2855-2867.https://doi.org/10.2147/DDDT.S111351
30.Miyake M, Anai S, Fujimoto K, Ohnishi S, Kuwada M, Nakai Y, et al. 5 fluorouracil enhances the antitumor effect of sorafenib and sunitinib in a xenograft model of human renal cell carcinoma. Oncol Let. 2012 Jun;3(6):1195-1202.https://doi.org/10.3892/ol.2012.662
31.Ma Y, Wang Y, Xu Z, Wang Y, Fallon JK, Liu F. Extreme low dose of 5-fluorouracil reverses MDR in cancer by sensitizing cancer associated fibroblasts and down-regulating P-gp. PLoS One. 2017 Jun 29;12(6):e0180023.https://doi.org/10.1371/journal.pone.0180023
32.Yang LQ, Lan YQ, Guo H, Cheng LZ, Fan JZ, Cai X, et al. Ophthalmic drug-loaded N,O-carboxymethyl chitosan hydrogels: synthesis, in vitro and in vivo evaluation. Acta Pharmacologica Sinica. 2010; 31: 1625-34;https://doi.org/10.1038/aps.2010.125
##submission.downloads##
Опубліковано
Як цитувати
Номер
Розділ
Ліцензія
Авторське право (c) 2025 Ю. М. Самченко, А. П. Малецький, Н. М. Бігун, Г. А. Долинський, Л.О. Керносенко, Н. О. Пасмурцева, Т. П. Полторацька, І. Є. Мамишев

Ця робота ліцензується відповідно до Creative Commons Attribution 4.0 International License.
Ця робота ліцензується відповідно до ліцензії Creative Commons Attribution 4.0 International (CC BY). Ця ліцензія дозволяє повторно використовувати, поширювати, переробляти, адаптувати та будувати на основі матеріалу на будь-якому носії або в будь-якому форматі за умови обов'язкового посилання на авторів робіт і первинну публікацію у цьому журналі. Ліцензія дозволяє комерційне використання.
ПОЛОЖЕННЯ ПРО АВТОРСЬКІ ПРАВА
Автори, які подають матеріали до цього журналу, погоджуються з наступними положеннями:
- Автори отримують право на авторство своєї роботи одразу після її публікації та назавжди зберігають це право за собою без жодних обмежень.
- Дата початку дії авторського права на статтю відповідає даті публікації випуску, до якого вона включена.
ПОЛІТИКА ДЕПОНУВАННЯ
- Редакція журналу заохочує розміщення авторами рукопису статті в мережі Інтернет (наприклад, у сховищах установ або на особистих веб-сайтах), оскільки це сприяє виникненню продуктивної наукової дискусії та позитивно позначається на оперативності і динаміці цитування.
- Автори мають право укладати самостійні додаткові угоди щодо неексклюзивного розповсюдження статті у тому вигляді, в якому вона була опублікована цим журналом за умови збереження посилання на первинну публікацію у цьому журналі.
- Дозволяється самоархівування постпринтів (версій рукописів, схвалених до друку в процесі рецензування) під час їх редакційного опрацювання або опублікованих видавцем PDF-версій.
- Самоархівування препринтів (версій рукописів до рецензування) не дозволяється.