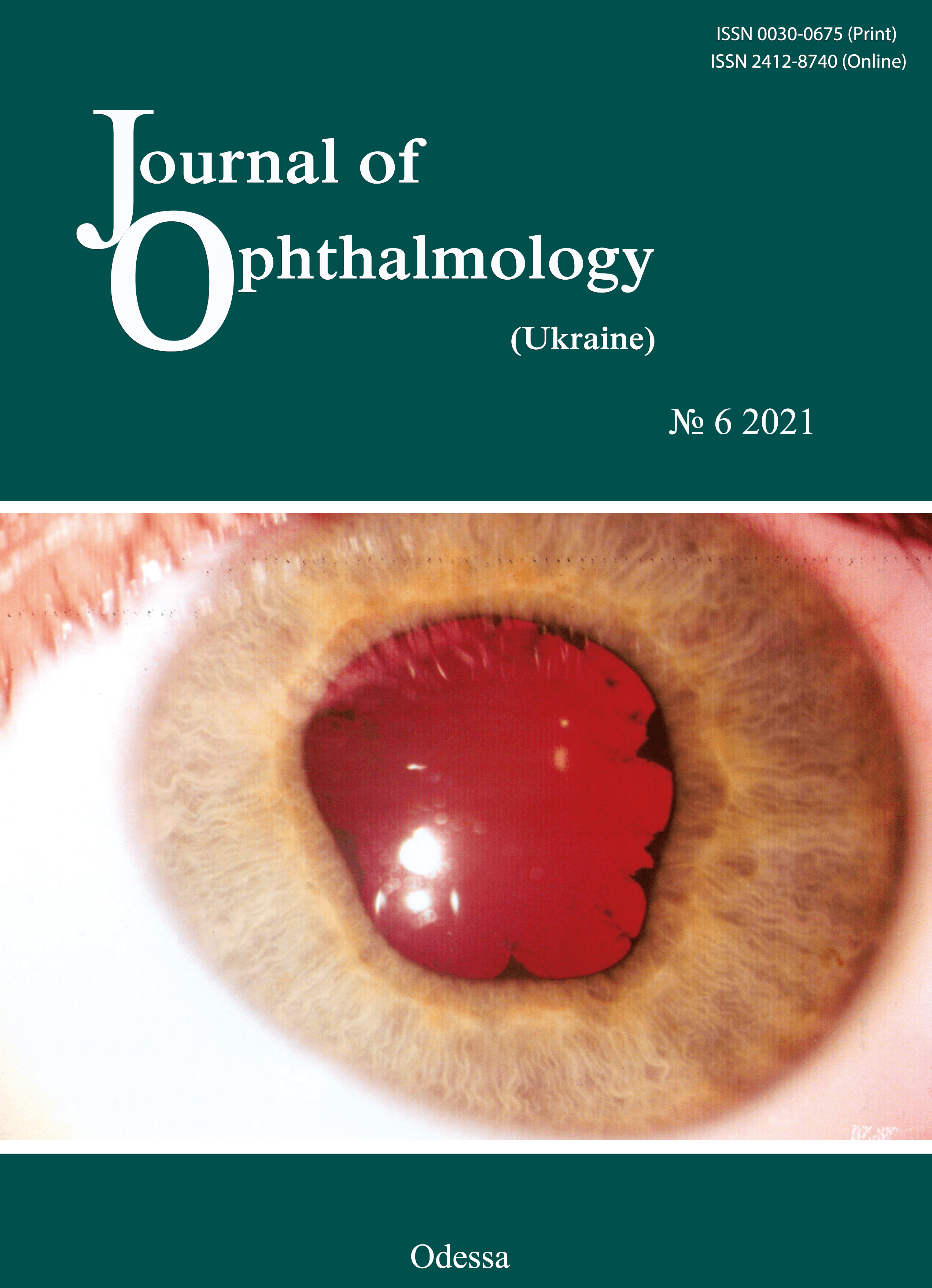
A case of persistent recurrent herpes zoster ophthalmicus in a patient with primary mannose binding lectin deficiency
DOI:
https://doi.org/10.31288/oftalmolzh202166468Keywords:
immunodiagnostics, immunotherapy, keratoconjunctivitis, corneal opacity, immunodeficiencyAbstract
In the current paper, we present an example case of persistent recurrent herpes zoster ophthalmicus with the development of chronic keratoconjunctivitis, corneal opacity, secondary eczema herpeticum and resistance both to antiviral drugs and to anti-allergic medications in a female patient with primary MBL deficiency. Particularly, we demonstrate how the elucidation of the causative immune deficiency and the related administration of specific replacement immunotherapy has become the cornerstone of the achievement of clinical success in the difficult-to-treat patient. Immunological tests demonstrated that the patient had a significantly reduced MBL level (167 ng/ml compared to a norm of 450 ng/ml), whereas other studied immune status characteristics where within normal range. We identified two pathological polymorphisms in the promoter and structural region of MBL-2 (particularly, –550 G/C and 221 C/G), which indicated that the patient had a primary MBL deficiency. It was the fact that the patient had the above genetic immunodeficiency disease that an atypical and unfavorable course of varicella zoster virus infection was associated in this case. The identification of primary MBL deficiency opened the door for new ways of therapy for the difficult-to-treat infectious disease through the specific replacement immunotherapy with the aim of improving immune control of the opportunistic agent through compensation of primary immunodeficiency.
References
1.Denier M, Gabison E, Sahyoun M, et al. Stromal Keratitis After Varicella in Children. Cornea. 2020 Jun;39(6):680-4.https://doi.org/10.1097/ICO.0000000000002281
2.Nofal A, Fawzy MM, Sharaf El Deen SM, El-Hawary EE. Herpes zoster ophthalmicus in COVID-19 patients. Int J Dermatol. 2020 Dec;59(12):1545-1546.https://doi.org/10.1111/ijd.15240
3.Maltsev DV. [Mannose binding lectin deficiency]. Ukrainskyi terapevtychnyi zhurnal. 2015; 1:80-9. Ukrainian.
4.Maltsev DV. [Cases of mannose binding lectin deficiency]. Ukrainskyi medychnyi chasopys. 2015;2 (106):122-7. Ukrainian.
5.Gao DN, Zhang Y, Ren YB, et al. Relationship of Serum Mannose-Binding Lectin Levels with the Development of Sepsis: a Meta-analysis. Inflammation. 2015 Feb;38(1):338-47.https://doi.org/10.1007/s10753-014-0037-5
6.de Morais VMS, de Lima ELS, Cahú GG, et al. MBL2 gene polymorphisms in HHV-8 infection in people living with HIV/AIDS. Retrovirology. 2018 Nov 27;15(1):75.https://doi.org/10.1186/s12977-018-0456-8
7.Lambourne J, Agranoff D, Herbrecht R, et al. Association of mannose-binding lectin deficiency with acute invasive aspergillosis in immunocompromised patients. Clin Infect Dis. 2009 Nov 15;49(10):1486-91.https://doi.org/10.1086/644619
8.Antony JS, Ojurongbe O, van Tong H, et al. Mannose-binding lectin and susceptibility to schistosomiasis. J Infect Dis. 2013. 2013 Jun 1;207(11):1675-83.https://doi.org/10.1093/infdis/jit081
9.Maltsev DV, Hurzhii OO. ANA-associated uveitis in the presence of reactivated HHV-7 infection in a patient with MBL deficiency. J Ophthalmol (Ukraine). 2020;6 (497):64-9.https://doi.org/10.31288/oftalmolzh202066469
10.Birbian N, Singh J, Jindal SK, et al. Association of the wild-type A/A genotype of MBL2 codon 54 with asthma in a North Indian population. Dis Markers. 2012;32(5):301-8. https://doi.org/10.1155/2012/757302
11.Eurich D, Boas-Knoop S, Morawietz L, et al. Association of mannose-binding lectin-2 gene polymorphism with the development of hepatitis C-induced hepatocellular carcinoma. Liver Int. 2011 Aug;31(7):1006-12.https://doi.org/10.1111/j.1478-3231.2011.02522.x
12.Vengen IT, Madsen HO, Garred P, et al. Mannose-binding lectin deficiency is associated with myocardial infarction: the HUNT2 study in Norway. PLoS One. 2012;7(7):e42113.https://doi.org/10.1371/journal.pone.0042113
13.Christiansen OB, Nielsen HS, Lund M, et al. Mannose-binding lectin-2 genotypes and recurrent late pregnancy losses. Hum Reprod. 2009 Feb;24(2):291-9.https://doi.org/10.1093/humrep/den377
14.Alstadhaug KB, Kvarenes HW, Prytz J, Vedeler C. A case of relapsing-remitting facial palsy and ipsilateral brachial plexopathy caused by HSV-1. J Clin Virol. 2016 May;78:62-5.https://doi.org/10.1016/j.jcv.2016.03.003
15.Tang YW, Cleavinger PJ, Li H, et al. Analysis of candidate-host immunogenetic determinants in herpes simplex virus-associated Mollaret's meningitis. Clin Infect Dis. 2000 Jan;30(1):176-8.https://doi.org/10.1086/313616
16.Friborg JT, Jarrett RF, Koch A, et al. Mannose-binding lectin genotypes and susceptibility to Epstein-Barr virus infection in infancy. Clin Vaccine Immunol. 2010 Sep;17(9):1484-7.https://doi.org/10.1128/CVI.00527-09
17.Manuel O, Pascual M, Trendelenburg M, Meylan PR. Association between mannose-binding lectin deficiency and cytomegalovirus infection after kidney transplantation. Transplantation. 2007 Feb 15;83(3):359-62.https://doi.org/10.1097/01.tp.0000251721.90688.c2
18.Valdimarsson H. Infusion of plasma-derived mannan-binding lectin (MBL) into MBL-deficient humans. Biochem Soc Trans. 2003 Aug;31(Pt 4):768-9.https://doi.org/10.1042/bst0310768
19.Garred P, Pressler T, Lanng S, et al. Mannose-binding lectin (MBL) therapy in an MBL-deficient patient with severe cystic fibrosis lung disease. Pediatr Pulmonol. 2002 Mar;33(3):201-7.https://doi.org/10.1002/ppul.10064
20.Frakking FN, Brouwer NM, van de Wetering D, et al. Safety and pharmacokinetics of plasma-derived mannose-binding lectin (MBL) substitution in children with chemotherapy-induced neutropaenia. Eur J Cancer. 2009 Mar;45(4):505-12.https://doi.org/10.1016/j.ejca.2008.11.036
21.Petersen KA, Matthiesen F, Agger T. Phase I safety, tolerability, and pharmacokinetic study of recombinant human mannan-binding lectin. J Clin Immunol. 2006 Sep;26(5):465-75.https://doi.org/10.1007/s10875-006-9037-z
22.Maltsev DV. [The effectiveness of cryopreserved human plasma replacement therapy in patients with primary mannose-binding lectin deficiency suffering from chronic active herpes virus infection]. Immunopatologiia, allergologiia i infektologiia. 2020;2:15-25. Russian.https://doi.org/10.14427/jipai.2020.2.15
23.Maltsev DV, Hurzhii OO. Toxoplasma chorioretinitis in primary myeloperoxidase MPO deficiency: A case report. J Ophthalmol (Ukraine). 2019;4:75-81.https://doi.org/10.31288/oftalmolzh201947581
Downloads
Published
How to Cite
Issue
Section
License
Copyright (c) 2025 Д. В. Мальцев

This work is licensed under a Creative Commons Attribution 4.0 International License.
This work is licensed under a Creative Commons Attribution 4.0 International (CC BY 4.0) that allows users to read, download, copy, distribute, print, search, or link to the full texts of the articles, or use them for any other lawful purpose, without asking prior permission from the publisher or the author as long as they cite the source.
COPYRIGHT NOTICE
Authors who publish in this journal agree to the following terms:
- Authors hold copyright immediately after publication of their works and retain publishing rights without any restrictions.
- The copyright commencement date complies the publication date of the issue, where the article is included in.
DEPOSIT POLICY
- Authors are permitted and encouraged to post their work online (e.g., in institutional repositories or on their website) during the editorial process, as it can lead to productive exchanges, as well as earlier and greater citation of published work.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work with an acknowledgement of its initial publication in this journal.
- Post-print (post-refereeing manuscript version) and publisher's PDF-version self-archiving is allowed.
- Archiving the pre-print (pre-refereeing manuscript version) not allowed.