Efficacy of topical N-acetylcysteine as a part of multicomponent treatment for severe dry eye syndrome
DOI:
https://doi.org/10.31288/oftalmolzh2020338Keywords:
severe dry eye syndrome, mucin, mucous thread, N-acetylcysteine, mucolyticAbstract
Background: According to Tear Film and Ocular Surface Society's Dry Eye Workshop II, the precorneal tear film plays a crucial role in moisturizing the corneal surface and allowing for an optically smooth corneal surface. In addition, as a result of imbalanced secretion of the muco-aqueous phase of the tear film, the mucin layer traps shed epithelial cells, inflammatory cells, and debris to form a mucous clot within the lower conjunctival fornix. Increased mucus viscosity prevents moving mucus away via the punctum, which contributes to the development of severe dry eye syndrome (DES). Our clinical experience argues that tear replacement therapy alone can be not enough in the treatment of severe DES. N-acetylcysteine (NAC), a collagenase inhibitor, has been widely employed clinically as a mucolytic agent. Foreign literature is scant on the use of NAC as an anti-inflammatory, mucolytic, detoxicant and anti-oxidative agent in the treatment of DES.
Purpose: To assess the efficacy of topical 5% N-acetylcysteine as a part of multicomponent treatment for severe DES associated with increased mucus production.
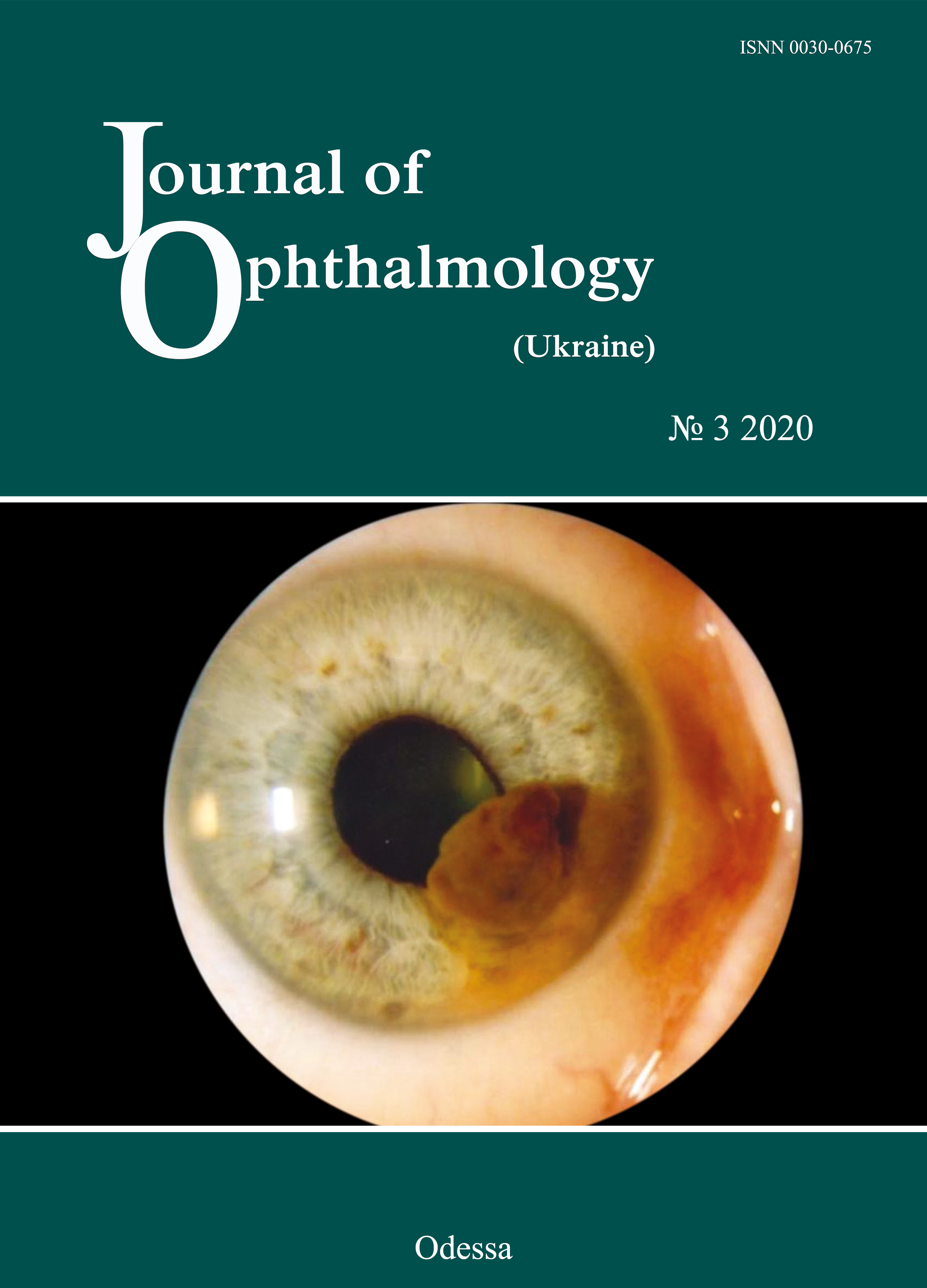
Material and Methods: We reviewed records of 15 patients examined and treated for severe DES. At baseline, there was biomicroscopic evidence of mucous discharge in the lower conjunctival fornix, corneal epitheliopathy in the form of punctate fluorescein staining, and desquamated epithelium, which was consistent with severe DES.
Results: At admission, mean Schirmer’s test value and tear break-up time (TBUT) were 3.4 mm (range, 2 to 6 mm) and 4.2 s (range, 2 to 8 s), respectively, and conjunctival impression cytology revealed focal epithelial degeneration. Topical 5% NAC was administered 4 times daily for 3 months as a part of multicomponent therapy for severe DES.
After 3 months of topical 5% NAC, 86.6% of patients noted good tolerance to the drug and improvement of subjective symptoms, and there was biomicroscopic evidence of a reduced amount of mucus in the lower conjunctival fornix and decreased epithelial desquamation. Mean Schirmer’s test and TBUT values increased to 5.0 ± 1.7 mm (mean ± SD) and 6.4 ± 1.7 s, respectively. Conjunctival impression cytology showed the presence of mucoid substance; diffused, differentiated epithelial cells without signs of degeneration; and an adequate superficial conjunctival epithelial cell layer.
Conclusion: Topical 5% N-acetylcysteine 4 times daily as a part of multicomponent treatment showed a substantial mucolytic effect for severe DES with apparent thick mucus discharge in the lower conjunctival fornix and resulted in the development of an adequate superficial conjunctival epithelial cell layer. Findings of this study allow us to recommend topical 5% N-acetylcysteine for severe DES patients with increased viscous mucous discharge in the lower conjunctival fornix.
References
1.Brzheskiĭ VV, Somov EE. [Corneal and conjunctival xerosis (diagnosis, clinical features, and management)]. 2nd ed. St Petersburg: Levsha; 2003. Russian.
2.Golubev SIu, Kuroiedov AV. [On the selection of economically efficacious agent for the prevention and treatment of dry eye syndrome]. Sindrom sukhogo glaza. 2002;3:12-4. Russian.
3.Egorov EA, Basinskii SN. [Clinical lectures on ophthalmology]. Moscow: GEOTAR; 2007. Russian.
4.Polunin GS, Polunina EG. [From dry eye to team film disease]. Oftalmologiia. 2012;9(2):4-7. Russian.
5.Bron AJ, de Paiva CS, Chauhan SK, Bonini S, Gabison EE, Jain S, et al. TFOS DEWS II Pathophysiology report. Ocul Surf. 2017;15:438-510.https://doi.org/10.1016/j.jtos.2017.05.011
6.Stapleton F, Alves M, Bunya VY, Jalbert I, Lekhanont K, Malet F, et al. TFOS DEWS II Epidemiology Report. Ocul Surf. 2017 Jul;15(3):334-365.https://doi.org/10.1016/j.jtos.2017.05.003
7.Vit VV. [Disorders of the eye, ocular adnexa and orbit], Vol. 1. Odesa: Astroprint; 2019. Russian.
8.Craig JP, Nichols KK, Akpek EK, Caffery B, Dua HS, Joo CK et al. TFOS DEWS II Definition and Classification Report. Ocul Surf. 2017 Jul;15(3):276-283.https://doi.org/10.1016/j.jtos.2017.05.008
9.Cheng K. H., Spanjaard L., Rutten H. et al. Immunoglobulin A antibodies against Pseudomonas aeruginosa in the tear fluid of contact lens wearers. Invest Ophthalmol Vis Sci. 1996. Vol. 37:2081-2088.
10.Little SA, Bruce AS. Postlens tear film morphology, lens movement and symptoms in hydrogel lens wearers. Ophthal Physiol Opt. 1994 Jan;14(1):65-9.https://doi.org/10.1111/j.1475-1313.1994.tb00559.x
11.Lowther GE. Dryness, Tears and Contact Lens Wear. Boston: Butterworth-Heinemann; 1997.
12.Ohashi Y, Motokura M, Kinoshita Y. Presence of epidermal growth factor in human tear. Invest Ophthalmol Vis Sci. 1989;30:1879-82.
13.Pucker AD, Ng SM, Nichols JJ. Over the counter (OTC) artificial tear drops for dry eye syndrome. Cochrane Database Syst Rev. 2016 Feb 23;2:CD009729.https://doi.org/10.1002/14651858.CD009729.pub2
14.Roth HW. Studies on the etiology and treatment of giant papillary conjunctivitis in contact lens wearers. Contactologia. 1991;13E:55-60.
15.Young G, Efron N. Characteristics of the pre-lens tear film during hydrogel contact lens wear. Ophthal Physiol Opt. 1991 Jan;11(1):53-8.https://doi.org/10.1111/j.1475-1313.1991.tb00195.x
16.Aragona P, Di Pietro R, Spinella R, Mobrici M. Conjunctival epithelium improvement after systemic pilocarpine in patients with Sjogren's syndrome. Br J Ophthalmol. 2006;90(2):166-70.https://doi.org/10.1136/bjo.2005.078865
17.Hamano H, Hori M, Hamano TA. A new method for measuring tears. CLAO J. 1983 Jul-Sep;9(3):281-9.
18.Somov EE. [Etiopathogenetic basic of dry eye syndrome and principles for an approach to treating the disease]. In: [Proceedings of Opthalmic Conference, Neva Horizons-2010]. Vol. 2. St Petersburg. October 15-16, 2010. Russian.
19.Downie LE, Keller PR. A pragmatic approach to dry eye diagnosis: evidence into practice. Optom Vis Sci. 2015;92(12):1189-97.https://doi.org/10.1097/OPX.0000000000000721
20.Ibrahim OM, Dogru M, Kawashima S, Wakamatsu TH, Tsubota K, Fujishima H. Visante optical coherence tomography and tear function test evaluation of cholinergic treatment response in patients with Sjogren syndrome. Cornea. 2013;32(5):653-7.https://doi.org/10.1097/ICO.0b013e318261eb4a
21.Petrone D, Condemi JJ, Fife R, Gluck O, Cohen S, Dalgin P. A double-blind, randomized, placebo-controlled study of cevimeline in Sjogren's syndrome patients with xerostomia and keratoconjunctivitis sicca. Arthritis Rheum. 2002;46(3):748-54.https://doi.org/10.1002/art.510
22.Wegener AR, Meyer LM, Schönfeld CL. Effect of viscous agents on corneal density in dry eye disease. J Ocul Pharmacol Ther. 2015 Oct;31(8):504-8.https://doi.org/10.1089/jop.2014.0157
23.Jordan A, Baum J. Basic tear flow: does it exist? Ophthalmology. 1980 Sep;87(9):920-30.https://doi.org/10.1016/S0161-6420(80)35143-9
24.Lemp MA. The mucin-deficient dry eye. Int Ophthalmol Clin. Int Ophthalmol Clin. 1973 Spring;13(1):185-9.https://doi.org/10.1097/00004397-197301310-00013
25.Somov EE, Brzheskiĭ VV. [Tear. Physiology, examination methods and clinical features]. St Petersburg: Nauka; 1994. Russian.
26.Albietz J, Sanfilippo P, Troutbeck R, Lenton LM. Management of filamentary keratitis associated with aqueous-deficient dry eye. Optom Vis Sci. 2003;80(6):420-30.https://doi.org/10.1097/00006324-200306000-00007
27.Inatomi T, Spurr-Michaud SJ, Tisdale AS, Gipson lK. Human corneal and conjunctival epithelia express MUC1 mucin. Invest Ophthalmol Vis Sci. 1995 Aug;36(9):1818-27.
28.Inatomi T, Spurr-Michaud SJ, Tisdale AS, Zhan Q, Feidman ST, Gipson IK. Expression of secretory mucin genes by human conjunctival epithelia. Invest Ophthalmol Vis Sci. 1996 Jul;37(8):1684-92.
29.Ralph RA. Conjunctival goblet cell density in normal subjects and in dry eye syndromes. Invest Ophthalmol. 1975;14(4):299-302.
30.Abreau K, Callan C, Kottaiyan R, Zhang A, Yoon G, Aquavella JV, et al. Temperatures of the Ocular Surface, Lid, and Periorbital Regions of Sjogren's, Evaporative, and Aqueous-Deficient Dry Eyes Relative to Normals. Ocul Surf. 2016;14:64-73.https://doi.org/10.1016/j.jtos.2015.09.001
31.Baudouin C, Messmer EM, AragonaJ P, Geerling G, Akova YA, Benitez-Del-Castillo J, et al. Revisiting the vicious circle of dry eye disease: a focus on the pathophysiology of meibomian gland dysfunction. Br J Ophthalmol. 2016;100:300-6.https://doi.org/10.1136/bjophthalmol-2015-307415
32.Kinoshita S, Kiorpes TC, Friend J, Thoft RA. Goblet cell density in ocular surface disease. A better indicator than tear mucin. Arch Ophthalmol. 1983;101:1284-7.https://doi.org/10.1001/archopht.1983.01040020286025
33.Pflugfelder SC, Tseng SC, Yoshino K, Monroy D, Felix C, Reis BL. Correlation of goblet cell density and mucosal epithelial membrane mucin expression with rose bengal staining in patients with ocular irritation. Ophthalmology. 1997;104:223-35.https://doi.org/10.1016/S0161-6420(97)30330-3
34.Corrales RM, de Paiva CS, Li DQ, Farley WJ, Henriksson JT, Bergmanson JP, et al. Entrapment of conjunctival goblet cells by desiccation-induced cornification. Invest Ophthalmol Vis Sci. 2011;52:3492-9.https://doi.org/10.1167/iovs.10-5782
35.Pflugfelder SC, Stern ME. Mucosal environmental sensors in the pathogenesis of dry eye. Expert Rev Clin Immunol. 2014;10:1137-40.https://doi.org/10.1586/1744666X.2014.944163
36.Shimazaki-Den S, Dogru M, Higa K, Shimazaki J. Symptoms, visual function, and mucin expression of eyes with tear film instability. Cornea. 2013 Sep;32(9):1211-8.https://doi.org/10.1097/ICO.0b013e318295a2a5
37.Zhang J, Yan X, Li H. Analysis of the correlations of mucins, inflammatory markers, and clinical tests in dry eye. Cornea. 2013 Jul;32(7):928-32.https://doi.org/10.1097/ICO.0b013e3182801622
38.Gipson IK. Distribution of mucins at the ocular surface. Exp Eye Res. 2004;78:379-88.https://doi.org/10.1016/S0014-4835(03)00204-5
39.Barabino S, Chen Y, Chauhan S, Dana R. Ocular surface immunity: homeostatic mechanisms and their disruption in dry eye disease. Prog Retin Eye Res. 2012;31:271-85.https://doi.org/10.1016/j.preteyeres.2012.02.003
40.Norn MS. Dead, degenerate, and living cells in conjunctival fluid and mucous thread. Acta Ophthalmol (Copenh). 1969;47:1102-15.https://doi.org/10.1111/j.1755-3768.1969.tb02509.x
41.Sheffner AL. The reduction in vitro in viscosity of mucoprotein solutions by a new mucolytic agent, N-acetyl-L-cysteine. Ann NY Acad Sci. 1963 Mar 30;106:298-310.https://doi.org/10.1111/j.1749-6632.1963.tb16647.x
42.Sakharov GM, Antonov NS. [Rendering care regarding tobacco dependence in therapeutic practice: A tutorial for physicians]. Moscow; 2010. Russian.
43.Baker WL, Anglade MW, Baker EL, White CM, Kluger J, Coleman CI. Use of N-acetylcysteine to reduce post-cardiothoracic surgery complications: a meta-analysis. Eur J Cardiothorac Surg. 2009 Mar;35(3):521-7.https://doi.org/10.1016/j.ejcts.2008.11.027
44.Kwok CS, Pang CL, Yeong JK, Loke YK. Measures used to treat contrast-induced nephropathy: overview of reviews. Br J Radiol. 2013 Jan; 86(1021):20120272.https://doi.org/10.1259/bjr.20120272
45.Inci I, Erne B, Arni S, Jungraithmayr W, Inci D, Hillinger S, et al. Prevention of primary graft dysfunction in lung transplantation by N-acetylcysteine after prolonged cold ischemia. J Heart Lung Transplant. 2010;29(11):1293-301.https://doi.org/10.1016/j.healun.2010.06.017
46.Borges-Santos MD, Moreto F, Pereira PC, Ming-Yu Y, Burini RC. Plasma glutathione of HIV⁺ patients responded positively and differently to dietary supplementation with cysteine or glutamine. Nutrition. 2012 Jul;28(7-8):753-6.https://doi.org/10.1016/j.nut.2011.10.014
47.Goossens N, Ditisheim S, Lanthier N, Spahr L, Hadengue A. [Alcoholic steatohepatitis: what's new in 2012?]. Rev Med. Suisse. 2012 Sep 5;8(352):1646-8, 1650-1. French.https://doi.org/10.53738/REVMED.2012.8.352.1646
48.Grant LM, Rockey DC. Drug-induced liver injury. Curr Opin Gastroenterol. 2012;28:198-202.https://doi.org/10.1097/MOG.0b013e3283528b5d
49.Müller, Svardal AM, Nordoy I, Berge RK, Aukrust P, Frøland SS. Virological and immunological effects of antioxidant treatment in patients with HIV infection. Eur J Clin Invest. 2000 Oct;30(10):905-14.https://doi.org/10.1046/j.1365-2362.2000.00727.x
50.Jones L. TFOS DEWS II Management and Therapy Report. Jones L, Downie LE, Korb D, Benitez-Del-Castillo JM, Dana R, Deng SX, et al. Ocul Surface. 2017 Jul;15(3):575-628.https://doi.org/10.1016/j.jtos.2017.05.006
51.Pokupec R, Petricek I, Sikic J, Bradic M, Popovic-Suic S, Petricek G. Comparison of local acetylcysteine and artificial tears in the management of dry eye syndrome. Acta Med Croat. 2005;59:337-40.
52.Pentapati M, Shah S. Filamentary keratitis: A case series. Int J Scientific Res Pub. 2015 Mar;5(3):1-7.
53.Ichikawa Y, Tokunaga M, Shimizu H, Moriuchi J, Takaya M, Arimori S. Clinical trial of ambroxol (Mucosolvan) in Sjögren's syndrome. Tokai J Exp Clin Med. 1988 Aug;13(3):165-9.
54.Kerksick C, Willoughby D. The antioxidant role of glutathione and N-acetylcysteine supplements and exercise-induced oxidative stress. J Int Soc Sports Nutr. 2005;2:38-44.https://doi.org/10.1186/1550-2783-2-2-38
Downloads
Published
How to Cite
Issue
Section
License
Copyright (c) 2025 О. Н. Иванова, Г. И. Дрожжина, Л. Ф. Тройченко, В. В. Вит, А. Б. Абрамова, Т. Д. Лотош

This work is licensed under a Creative Commons Attribution 4.0 International License.
This work is licensed under a Creative Commons Attribution 4.0 International (CC BY 4.0) that allows users to read, download, copy, distribute, print, search, or link to the full texts of the articles, or use them for any other lawful purpose, without asking prior permission from the publisher or the author as long as they cite the source.
COPYRIGHT NOTICE
Authors who publish in this journal agree to the following terms:
- Authors hold copyright immediately after publication of their works and retain publishing rights without any restrictions.
- The copyright commencement date complies the publication date of the issue, where the article is included in.
DEPOSIT POLICY
- Authors are permitted and encouraged to post their work online (e.g., in institutional repositories or on their website) during the editorial process, as it can lead to productive exchanges, as well as earlier and greater citation of published work.
- Authors are able to enter into separate, additional contractual arrangements for the non-exclusive distribution of the journal's published version of the work with an acknowledgement of its initial publication in this journal.
- Post-print (post-refereeing manuscript version) and publisher's PDF-version self-archiving is allowed.
- Archiving the pre-print (pre-refereeing manuscript version) not allowed.